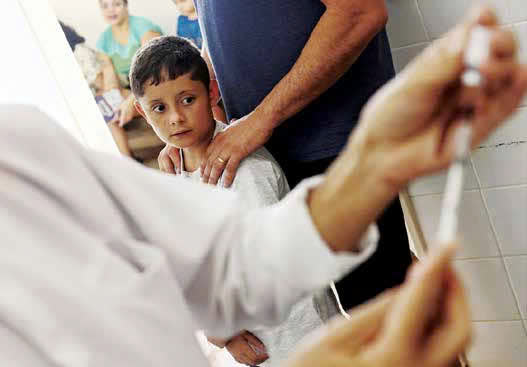
Chích ngừa vaccine sốt xuất huyết cho trẻ em Brazil, nơi bùng phát mạnh bệnh này. Ảnh: Science
Vaccine do Bộ Y tế cấp phép có tên Qdenga do công ty dược phẩm Takeda (Nhật Bản) sản xuất. Qdenga sử dụng một chủng virus Dengue D2 sống đã được giảm độc lực (live attenuated) có tên gọi DENV-2 PDK-53 strain (TDV- 2) và những virus thuộc type D1, D3, D4; dựa trên cấu trúc TDV2 đã được thay thế các gene prM và E bằng các gene tương ứng của ba virus còn lại
Như vậy vaccine Qdenga là vaccine đa giá (polyvalent) có khả năng chống lại cả 4 type virus sốt xuất huyết Dengue gây bệnh. Tuy còn sống nhưng các virus tạo thành vaccine này không gây bệnh, chỉ giúp hệ miễn dịch cơ thể sản xuất các kháng thể chống lại virus Dengue.
Kết quả thử nghiệm lâm sàng Qdenga như thế nào?
Qua thử nghiệm trên 20.000 trẻ em tuổi từ 4 - 16 tuổi tại 8 quốc gia Châu Mỹ Latinh và Châu Á Thái Bình Dương, Qdenga giúp giảm được 80% các trường hợp sốt gây ra bởi nhiễm virus Dengue trên những trẻ đã được tiêm chủng 2 mũi cách nhau 12 tháng: 61/12.700 trẻ sử dụng Qdenga so với 149/6.318 trẻ tiêm giả dược (placebo).
Ngoài ra sau khi tiêm 18 tháng, Qdenga còn giúp giảm 90% trường hợp nhập viện: 13/12.700 (0.1%) so với 66/6.316 (1%) nhóm chứng.
Trong nhóm chưa bao giờ bị nhiễm virus Dengue (huyết thanh âm tính) các nhà nghiên cứu ghi nhận hiệu lực rõ ràng đối với type huyết thanh D1 và D2, không rõ đối với D3 và không thể kết luận với D4 (vì số lượng bệnh nhân quá ít).
Sau 22 - 27 tháng theo dõi sau mũi tiêm đầu tiên, phản ứng không mong muốn trầm trọng (SAE) là 5% (664/13.380) ở nhóm tiêm vaccine và 5.9% (396/6.687) ở nhóm chứng. Có 17 trường hợp tử vong (11:6), nhưng tất cả đều không liên quan đến vaccine.
Các phản ứng không mong muốn khác gồm: đau chỗ chích (50%), nhức đầu(35%), đau cơ (31%), chỗ tiêm sưng đỏ (27%), cảm giác khó chịu (24%), mệt mỏi (20%), sốt (11%). Nhiều phản ứng khác với tỷ lệ 10% cũng ghi nhận như viêm họng, ngứa, nổi mẫn đỏ.
Đối với vấn đề ‘tăng nặng phụ thuộc vào kháng thể’ (Antibody dependent-enhancement - ADE), do hiệu quả cao hơn cho cả 4 type virus Dengue cùng nhiều cải tiến kỹ thuật, nên vaccine Qdenga có lẽ giảm được nguy cơ ADE qua số liệu SAE theo dõi (gồm cả đối tượng ĐÃ và CHƯA bị sơ nhiễm virus Dengue)
Qdenga được chấp nhận ra sao?
Hiện tại Tổ chức Y tế thế giới (WHO) đã cho phép tạm thời sử dụng (pre-qualified) Qdenga cho trẻ từ 6 - 16 tuổi ở vùng lưu hành Dengue CAO, nghĩa là vùng có hơn 60% trẻ dưới 9 tuổi có kháng thể Dengue hoặc vùng có trẻ nhập viện vì Dengue cao nhất là nhóm dưới 16 tuổi.
Theo WHO, cần chờ số liệu rõ ràng về nguy cơ và lợi ích của nhóm chưa bị nhiễm D3 và D4 thì mới quyết định có khuyến cáo sử dụng vaccine Qdenga cho vùng lưu hành Dengue nhẹ và trung bình. Với người mắc nhiều bệnh khác thì giới hạn tuổi là từ 6 - 60 tuổi.
Phụ nữ mang thai, người cho con bú, mắc bệnh suy giảm miễn dịch bẩm sinh hay mắc phải, hoặc sử dụng thuốc ức chế miễn dịch thì không được tiêm phòng Qdenga.
Những nơi nào đã phê duyệt Qdenga?

Nhà máy sản xuất vaccine Qdenga tại Đức. Ảnh: Takeda
Cơ quan quản lý thuốc Châu Âu (European Medicines Agency - EMA) đã chấp nhận Qdenga với lý do xét thấy lợi ích cao hơn nguy cơ trong phòng ngừa chống 4 type virus Dengue và theo chỉ định của nhà sản xuất.
Ngược lại, Cơ quan Quản lý thực phẩm và Thuốc (FDA) Hoa Kỳ chưa phê duyệt Qdenga vì yêu cầu bổ sung số liệu từ những người sốt nhưng không nhập viện sau tiêm chủng vaccine. Vào tháng 11-2023, Takeda đã tự nguyện rút đơn xin phê duyệt lại.
Các nước đã phê duyệt Qdenga gồm Indonesia, Thái Lan, Malaysia, Anh, Brazil, Argentina, các nước châu Âu (qua EMA). Công ty cũng đang tiến hành thủ tục phê duyệt vaccine tại Ấn Độ. Đa số các nước trên đều là vùng Dengue lưu hành nặng ngoại trừ châu Âu. Việt Nam cũng đã phê duyệt Qdenga vào tháng 5-2024 và cho triển khai tiêm chủng.
Ba “thế hệ” vaccine Dengue
- CYD-TDV (Denguevaxia): Do tập đoàn dược phẩm Sanofi Pasteur sản xuất, dựa trên cấu trúc virus Sốt vàng (Yellow Fever). Vaccine này dùng virus sống giảm độc lực, tiêm 3 mũi, được FDA và WHO cho phép lưu hành. Chỉ định tiêm phòng cho người từ 9 - 45 tuổi. Nhưng do vaccine có thể gây bệnh nặng hơn sau khi tiêm chủng cho người chưa sơ nhiễm nên chỉ định bị giới hạn và hiện nay Sanofi Pasteur cũng đã ngừng sản xuất.
- TAK-003 (Qdenga): Sản phẩm của Takeda, cũng là vaccine dùng virus sống giảm độc lực trên nền virus Dengue 2. Chỉ định tiêm 2 mũi cách nhau 3 tháng cho người từ 4 tuổi trở lên, bất kể đã bị sơ nhiễm hay chưa. Như nói ở trên, vaccine được EMA, WHO và nhiều nước có dịch SXH-Dengue chấp nhận.
- Butantan–Dengue Vaccine (ButantanDV): Vaccine do Viện Truyền nhiễm và Dị ứng Hoa Kỳ (NIAID) phát triển đang thử nghiệm giai đoạn 3 ở Brazil.
| TÌNH HÌNH SỐT XUẤT HUYẾT DENGUE TRÊN THẾ GIỚI Tính đến tháng 5 năm nay WHO ghi nhận đã có hơn 7,6 triệu ca sốt xuất huyết trong năm 2024, gồm 3,4 triệu ca được xác nhận, hơn 16.000 ca nặng và hơn 3.000 ca tử vong. Sốt xuất huyết tăng mạnh ở châu Mỹ, nơi vào cuối tháng 4-2024 đã có 7 triệu ca mắc, vượt qua con số 4,6 triệu ca mắc của cả năm 2023. Trong 50 năm qua, tỷ lệ mắc sốt xuất huyết tăng 30 lần. Ước tính mỗi năm có 50 – 100 triệu ca mắc. Hiện tại có hơn 100 quốc gia ghi nhận có sốt xuất huyết. |
|---|
Kết quả ban đầu công bố trên tạp chí The New England Journal of Medicine vào tháng 2-2024 ghi nhận: Thử nghiêm trên 16.235 người tình nguyện từ 2 - 59 tuổi cho thấy chỉ cần một liều duy nhất.
Sau 2 năm theo dõi, vaccine Butantan DV có thể phòng ngừa triệu chứng của các virus Dengue type 1 và 2 với tỷ lệ 80% bất kể người đã hoặc chưa bị sơ nhiễm. Vì ít bệnh nhân nên với D3 và D4 chưa kết luận được. Kết quả củng cố thêm hiệu lực của vaccine này trên trẻ em và người lớn.
Hiện nay cũng có khá nhiều nghiên cứu về vaccine Dengue với kỹ thuật mRNA đang được tiến hành. Hy vọng một ngày không xa con người sẽ có thêm nhiều vaccine phòng ngừa sốt xuất huyết Dengue hiệu quả, qua đó góp phần khống chế căn bệnh nhiễm trùng nguy hiểm này.
![[Banner Top] Medlaw](/uploads/a7259844-bfd9-4875-9a6c-a7f560b6be97.jpg)
![[Banner Top] Hồng Phát](/uploads/88dbe592-ac75-433d-94aa-d42b69ff5a0c.jpg)
![[Banner Top] Nest Insight](/uploads/88b8a614-6e94-4782-9408-36644eead85d.jpg)

![[Banner Mid] Hồng Phát](/uploads/0a12ba57-9f3d-4828-94da-cf937789b409.jpg)














![[Banner Side] Medlaw](/uploads/b729448e-c98e-455a-9d7a-9e658c271f5b.jpg)
Ý kiến của bạn
{% item.name %}
{% item.comment %}